Purina

| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
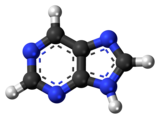
9H-purina
| |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.004.020 |
| KEGG | |
| MeSH | Purine |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C5H4N4 | |
| Jisim molar | 120.12 g·mol−1 |
| Takat lebur | 214 °C (417 °F; 487 K) |
| 500 g/L (RT) | |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Purina ialah sebatian organik aromatik sebatian heterokitar yang terdiri daripada dua cincin (pirimidina dan imidazola) yang bercantum. Ia larut dalam air. Purina juga merupakan nama kelas molekul yang lebih luas, yang termasuk purina tersubstitusi dan tautomernya. Mereka adalah heterokitar yang mengandungi nitrogen yang paling banyak terdapat dalam alam semula jadi.[1]
Sumber pemakanan
[sunting | sunting sumber]Purin didapati dalam kepekatan tinggi dalam daging dan produk daging, terutamanya organ dalaman seperti hati dan buah pinggang. Secara amnya, diet berasaskan tumbuhan adalah rendah purina.[2] Tumbuhan purina tinggi dan alga termasuk beberapa kekacang (lentil dan kacang tunggak) dan spirulina. Contoh sumber purina tinggi termasuk: roti manis, ikan bilis, sardin, hati, buah pinggang daging lembu, otak, ekstrak daging (cth. Oxo, Bovril), hering, makarel, kerang, daging buruan, yis (bir, ekstrak yis, yis pemakanan) dan kuah.[3]
Jumlah purina yang sederhana juga terkandung dalam daging merah, daging lembu, daging babi, ayam itik, ikan dan makanan laut, asparagus, kubis bunga, bayam, cendawan, kacang hijau, lentil, kacang polong kering, kacang, oatmeal dan gandum.[4]
Biokimia
[sunting | sunting sumber]Purina dan pirimidina membentuk dua kumpulan bes nitrogen, termasuk dua kumpulan bes nukleotida. Bes purina ialah guanina (G) dan adenina (A) yang membentuk nukleosida yang sepadan- deoksiribonukleosida (deoksiguanosina dan deoksiadenosina) dengan bahagian deoksiribosa dan ribonukleosida (guanosina, adenosina) dengan bahagian ribosa. Nukleosida dengan asid fosforik ini membentuk nukleotida yang sepadan (deoksiguanilat, deoksiadenilat dan guanilat, adenilat) yang menjadi blok binaan DNA dan RNA, masing-masing. Bes purina juga memainkan peranan penting dalam banyak proses metabolik dan isyarat dalam sebatian guanosina monofosfat (GMP) dan adenosina monofosfat (AMP).
Untuk melaksanakan proses selular penting ini, kedua-dua purina dan pirimidina diperlukan oleh sel, dan dalam kuantiti yang sama. Kedua-dua purina dan pirimidina adalah perencat dan pengaktif diri. Apabila purina terbentuk, ia menghentikan enzim yang diperlukan untuk menghasilkan lebih banyak purina. Perencatan diri ini berlaku kerana ia juga mengaktifkan enzim yang diperlukan dalam pembentukan pirimidina. Pirimidina secara serentak menghalang diri dan mengaktifkan purina dengan cara yang sama. Oleh kerana itu, terdapat hampir jumlah yang sama kedua-dua bahan dalam sel pada setiap masa.[5]
Sifat
[sunting | sunting sumber]Purin ialah kedua-dua asid yang sangat lemah (pKa 8.93) dan juga bes yang lebih lemah (pKa 2.39).[6] Jika dilarutkan dalam air tulen, pH adalah separuh antara kedua-dua nilai pKa ini.
Purina adalah aromatik, mempunyai empat tautomer setiap satu dengan hidrogen yang terikat pada satu yang berbeza daripada empat atom nitrogen. Ini dikenal pasti sebagai 1-H, 3-H, 7-H, dan 9-H (lihat imej cincin bernombor). Bentuk kristal biasa memihak kepada tautomer 7-H, manakala dalam pelarut polar kedua-dua tautomer 9-H dan 7-H mendominasi.[7] Substituen kepada cincin dan interaksi dengan molekul lain boleh mengalihkan keseimbangan tautomer ini.[8]
Purina utama
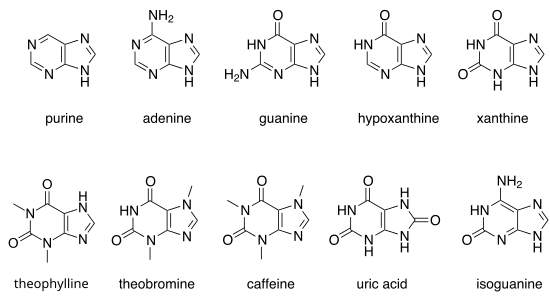
[sunting | sunting sumber]Terdapat banyak purina semula jadi. Ia termasuk nukleobes adenina (2) dan guanina ( 3 ). Dalam DNA, bes ini membentuk ikatan hidrogen dengan pirimidina pelengkap, timina dan sitosina, masing-masing. Ini dipanggil pasangan asas pelengkap. Dalam RNA, pelengkap adenina ialah urasil dan bukannya berbanding.
Purin lain yang ketara ialah hipoxantina, xantina, teofilina, teobromina, kafeina, asid urik dan isoguanina.
Fungsi
[sunting | sunting sumber]
Selain daripada peranan penting purina (adenina dan guanina) dalam DNA dan RNA, purina juga merupakan komponen penting dalam beberapa biomolekul penting lain seperti ATP, GTP, AMP kitaran, NADH dan koenzim A. Purina (1) itu sendiri, tidak dijumpai secara semula jadi semula jadi, tetapi ia boleh dihasilkan melalui sintesis organik.
Mereka juga boleh berfungsi secara langsung sebagai neurotransmiter, bertindak ke atas reseptor purinergik. Adenosin mengaktifkan reseptor adenosina.
Sejarah
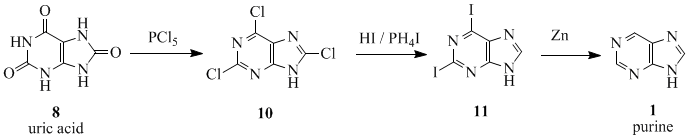
[sunting | sunting sumber]Perkataan purina (asal pure urine, "kencing tulen") [9] dicipta oleh ahli kimia Jerman Emil Fischer pada tahun 1884.[10][11] Beliau mensintesiskannya buat kali pertama pada tahun 1898.[11] Bahan permulaan jujukan tindak balas ialah asid urik (8), yang telah diasingkan daripada batu karang oleh Carl Wilhelm Scheele pada 1776.[12] Asid urik telah bertindak balas dengan PCl5 untuk memperoleh 2,6,8-trikloropurina (10), yang ditukar dengan HI dan PH4I untuk memberikan 2,6-diiodopurina (11). Produk telah diturunkan menjadi purina (1) menggunakan serbuk zink.
Metabolisme
[sunting | sunting sumber]Banyak organisma mempunyai laluan metabolik untuk mensintesis dan memecahkan purin.
Purin disintesis secara biologi sebagai nukleosida (asas yang melekat pada ribosa).
Pengumpulan nukleotida purina yang diubah suai adalah rosak kepada pelbagai proses selular, terutamanya yang melibatkan DNA dan RNA. Untuk berdaya maju, organisma mempunyai sejumlah deoksipurina fosfohidrolase yang menghidrolisis terbitan purina ini dengan menyingkirkannya daripada kumpulan NTP dan dNTP yang aktif. Deaminasi bes purina boleh mengakibatkan pengumpulan nukleotida seperti ITP, dITP, XTP dan dXTP.[13]
Kecacatan pada enzim yang mengawal pengeluaran dan pemecahan purina boleh mengubah jujukan DNA sel dengan teruk, yang mungkin menjelaskan mengapa orang yang membawa varian genetik tertentu enzim metabolik purina mempunyai risiko yang lebih tinggi untuk beberapa jenis kanser.
Biosintesis dalam tiga domain kehidupan
[sunting | sunting sumber]Organisma dalam ketiga-tiga domain kehidupan – eukariot, bakteria dan arkea – mampu menjalankan biosintesis de novo purin. Keupayaan ini mencerminkan keperluan purina untuk kehidupan. Laluan biokimia sintesis sangat serupa dalam eukariot dan spesies bakteria, tetapi lebih berubah-ubah di kalangan spesies arkea.[14] Satu set gen yang hampir lengkap, atau lengkap, yang diperlukan untuk biosintesis purina telah ditentukan hadir dalam 58 daripada 65 spesies arkea yang dikaji.[14] Walau bagaimanapun, turut dikenal pasti ialah tujuh spesies arkea dengan tiada atau hampir tiada gen pengekodan purina. Rupa-rupanya, spesies arkea yang tidak dapat mensintesis purina dapat memperoleh purina eksogen untuk pertumbuhan,[14] dan dengan itu, beranalog dengan mutan purina eukariot seperti mutan purina kulat Neurospora crassa[15] yang juga memerlukan purina eksogen dalam pertumbuhan.
Hubungan dengan gout
[sunting | sunting sumber]Tahap penggunaan daging dan makanan laut yang lebih tinggi dikaitkan dengan peningkatan risiko gout, manakala tahap penggunaan produk tenusu yang lebih tinggi dikaitkan dengan penurunan risiko. Pengambilan sederhana sayur-sayuran atau protein yang kaya dengan purina tidak dikaitkan dengan peningkatan risiko gout.[16] Keputusan yang sama telah ditemui dengan risiko hiperurisemia.
Sintesis makmal
[sunting | sunting sumber]Sebagai tambahan kepada sintesis purina in vivo dalam metabolisme purina, ia juga boleh dicipta secara buatan.
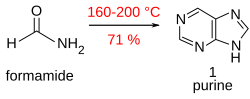
Purina (1) diperolehi dalam hasil yang baik apabila formamid dipanaskan dalam bekas terbuka pada suhu 170 °C selama 28 jam.[17]
Reaksi yang luar biasa ini dan lain-lain sepertinya telah dibincangkan dalam konteks asal-usul kehidupan.[18]
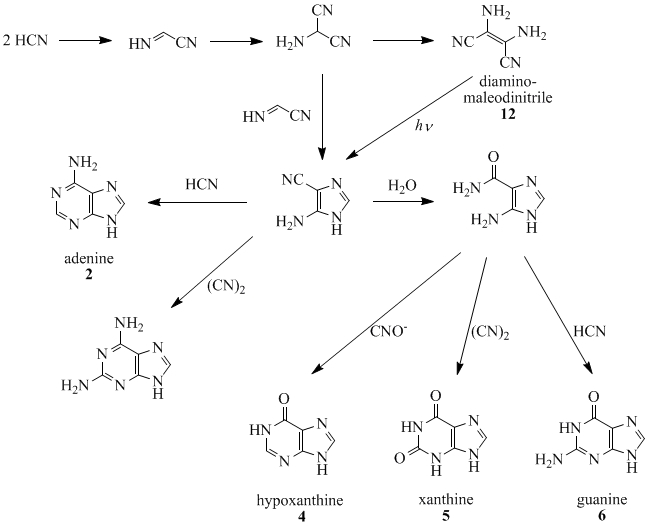
Oro, Orgel dan rakan sekerja telah menunjukkan bahawa empat molekul HCN bergabung untuk membentuk diaminomaleonitril (12), yang boleh ditukar kepada hampir semua purina semula jadi.[19][20][21][22][23] Sebagai contoh, lima molekul HCN terpeluwap dalam tindak balas eksotermik lalu menghasilkan adenina, terutamanya dengan kehadiran ammonia.
Sintesis purina Traube (1900) ialah tindak balas klasik (dinamakan sempena Wilhelm Traube) antara pirimidina digantikan amina, dan asid formik.[24]
Sintesis prebiotik
[sunting | sunting sumber]Untuk memahami bagaimana terbitnya kehidupan, pengetahuan diperlukan tentang laluan kimia yang membenarkan pembentukan blok binaan utama kehidupan di bawah keadaan prebiotik yang munasabah. Nam et al.[25] menunjukkan pemeluwapan langsung nukleobes purina dan pirimidina dengan ribosa untuk memberikan ribonukleosida dalam mikrotitisan akueus, satu langkah penting yang membawa kepada pembentukan RNA. Juga, proses prebiotik yang munasabah untuk mensintesis ribonukleosida purina telah dibentangkan oleh Becker et al.[26]
Rujukan
[sunting | sunting sumber]- ^ "The chemodiversity of purine as a constituent of natural products". Chemistry & Biodiversity. 1 (3): 361–401. March 2004. doi:10.1002/cbdv.200490033. PMID 17191854.
- ^ "Gout: List of Foods High and Low in Purine Content". Dietaryfiberfood.com. 2016-04-08. Diarkibkan daripada yang asal pada 2011-11-12. Dicapai pada 2016-07-16.
- ^ "Total purine and purine base content of common foodstuffs for facilitating nutritional therapy for gout and hyperuricemia". Biological & Pharmaceutical Bulletin. 37 (5): 709–721. 2014. doi:10.1248/bpb.b13-00967. PMID 24553148.
- ^ "Gout Diet: What Foods To Avoid". Healthcastle.com. Diarkibkan daripada yang asal pada 2017-08-14. Dicapai pada 2016-07-16.
- ^ Guyton AC (2006). Textbook of Medical Physiology. Philadelphia, PA: Elsevier. m/s. 37. ISBN 978-0-7216-0240-0.
- ^ Seela F, dll. (2014). Schaumann E (penyunting). Houben-Weyl Methods of Organic Chemistry. E 9b/2 (ed. 4th Supplement: Hetarenes III (Six-Membered Rings and Larger Hetero-Rings with Maximum Unsaturation) - Part 2b). m/s. 310. ISBN 9783131815040. Diarkibkan daripada yang asal pada 2022-02-17. Dicapai pada 2020-05-15.
- ^ "Purine tautomeric preferences and bond-length alternation in relation with protonation-deprotonation and alkali metal cationization". Journal of Molecular Modeling. 26 (5): 93. April 2020. doi:10.1007/s00894-020-4343-6. PMC 7256107. PMID 32248379.
- ^ "Effect of the H-bonding on aromaticity of purine tautomers". The Journal of Organic Chemistry. 77 (8): 4035–4045. April 2012. doi:10.1021/jo300406r. PMID 22448684.
- ^ McGuigan H (1921). An Introduction To Chemical Pharmacology. P. Blakiston's Sons & Co. m/s. 283. Diarkibkan daripada yang asal pada April 16, 2020. Dicapai pada July 18, 2012.
- ^ "Ueber die Harnsäure. I." [On uric acid. I.]. Berichte der Deutschen Chemischen Gesellschaft. 17: 328–338. 1884. doi:10.1002/cber.18840170196. Diarkibkan daripada yang asal pada 2021-01-18. Dicapai pada 2016-04-20.

From p. 329 Diarkibkan 2022-02-17 di Wayback Machine: "Um eine rationelle Nomenklatur der so entstehenden zahlreichen Substanzen zu ermöglichen, betrachte ich dieselben als Abkömmlinge der noch unbekannten Wasserstoffverbindung CH3.C5N4H3 and nenne die letztere Methylpurin." (In order to make possible a rational nomenclature for the numerous existing substances, I regarded them as derivatives of a still unknown hydrogen compound, CH3.C5N4H3, and call the latter "methylpurine".) - ^ a b "Ueber das Purina und seine Methylderivate" [On purine and its methyl derivatives]. Berichte der Deutschen Chemischen Gesellschaft. 31 (3): 2550–2574. 1898. doi:10.1002/cber.18980310304. Diarkibkan daripada yang asal pada 2020-10-18. Dicapai pada 2016-04-20.

From p. 2550 Diarkibkan 2020-10-18 di Wayback Machine: "…hielt ich es für zweckmäßig, alle diese Produkte ebenso wie die Harnsäure als Derivate der sauerstofffreien Verbindung C5H4N4 zu betrachten, und wählte für diese den Namen Purin, welcher aus den Wörtern purum und uricum kombiniert war." (…I regarded it as expedient to consider all of these products, just like uric acid, as derivatives of the oxygen-free compound C5H4N4, and chose for them the name "purine", which was formed from the [Latin] words purum and uricum.) - ^ "Examen chemicum calculi urinari" [A chemical examination of kidney stones]. Opuscula. 2: 73. 1776.
- ^ "Characterisation of multiple substrate-specific (d)ITP/(d)XTPase and modelling of deaminated purine nucleotide metabolism". BMB Reports. 45 (4): 259–264. April 2012. doi:10.5483/BMBRep.2012.45.4.259. PMID 22531138.
- ^ a b c Brown, Anne M.; Hoopes, Samantha L.; White, Robert H.; Sarisky, Catherine A. (2011). "Purine biosynthesis in archaea: Variations on a theme". Biology Direct. 6: 63. doi:10.1186/1745-6150-6-63. PMC 3261824. PMID 22168471.
- ^ Bernstein, H. (1961). "Imidazole Compounds Accumulated by Purine Mutants of Neurospora crassa". Journal of General Microbiology. 25: 41–46. doi:10.1099/00221287-25-1-41.
- ^ "Purine-rich foods, dairy and protein intake, and the risk of gout in men". The New England Journal of Medicine. 350 (11): 1093–1103. March 2004. doi:10.1056/NEJMoa035700. PMID 15014182.
- ^ "A One-step Synthesis of Purine Ring from Formamide". Chemical & Pharmaceutical Bulletin. 20 (3): 623. 1972. doi:10.1248/cpb.20.623. Diarkibkan daripada yang asal pada 2016-05-16.
- ^ "About a formamide-based origin of informational polymers: syntheses of nucleobases and favourable thermodynamic niches for early polymers". Origins of Life and Evolution of the Biosphere. 36 (5–6): 523–531. December 2006. Bibcode:2006OLEB...36..523S. doi:10.1007/s11084-006-9053-2. PMID 17136429.
- ^ "Studies in prebiotic synthesis. II. Synthesis of purine precursors and amino acids from aqueous hydrogen cyanide". Journal of Molecular Biology. 30 (2): 223–253. December 1967. doi:10.1016/S0022-2836(67)80037-8. PMID 4297187.
- ^ "An Unusual Photochemical Rearrangement in the Synthesis of Adenine from Hydrogen Cyanide". Journal of the American Chemical Society. 88 (5): 1074. March 1966. doi:10.1021/ja00957a050.
- ^ "Photochemical reactions and the chemical evolution of purines and nicotinamide derivatives". Science. 166 (3906): 765–766. November 1969. Bibcode:1969Sci...166..765F. doi:10.1126/science.166.3906.765. PMID 4241847.
- ^ "Amino-acid synthesis from hydrogen cyanide under possible primitive earth conditions". Nature. 190 (4774): 442–443. April 1961. Bibcode:1961Natur.190..442O. doi:10.1038/190442a0. PMID 13731262.
- ^ Bauer W (1985). Houben-Weyl Methods of Organic Chemistry Vol. E 5, 4th Edition Supplement. Thieme Georg Verlag. m/s. 1547. ISBN 9783131811547.
- ^ Hassner A, Stumer C (2002). Organic Syntheses Based on Name Reactions (ed. 2nd). Elsevier. ISBN 0-08-043259-X.
- ^ Nam I, Nam HG, Zare RN. Abiotic synthesis of purine and pyrimidine ribonucleosides in aqueous microdroplets. Proc Natl Acad Sci U S A. 2018 Jan 2;115(1):36-40. doi: 10.1073/pnas.1718559115. Epub 2017 Dec 18. PMID 29255025; PMCID: PMC5776833
- ^ Becker S, Thoma I, Deutsch A, Gehrke T, Mayer P, Zipse H, Carell T. A high-yielding, strictly regioselective prebiotic purine nucleoside formation pathway. Science. 2016 May 13;352(6287):833-6. doi: 10.1126/science.aad2808. PMID 27174989.