Indium(III) oksida
Penampilan
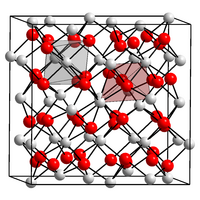
| |
| Nama | |
|---|---|
| Nama lain
Indium trioksida, indium seskuioksida
| |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChemSpider | |
| ECHA InfoCard | 100.013.813 |
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| In2O3 | |
| Jisim molar | 277.64 g/mol |
| Rupa bentuk | Hablur hijau kekuningan |
| Ketumpatan | 7.179 g/cm3 |
| Takat lebur | 1,910 °C (3,470 °F; 2,180 K) |
| Tidak larut | |
| Luang jalur | ~3 eV (300 K) |
| −56.0·10−6 cm3/mol | |
| Struktur | |
| Struktur kristal | Kubik, kumpulan ruang Ia3 No. 206, cI80, a = 1.0117(1) nm, Z = 16[1] |
| Bahaya | |
| Pengelasan EU | {{{value}}} |
| NFPA 704 (berlian api) | |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Indium(III) oksida merujuk kepada sebatian kimia indium dengan sebatian kimia In2O3. Sebatian ini merupakan sebatian oksida amfoterik.
Penghasilan
[sunting | sunting sumber]Indium(III) oksida pukal boleh dihasilkan melalui pemanasan indium(III) hidroksida, nitrat, karbonat atau sulfat.[2]
Tindak balas
[sunting | sunting sumber]Pada 700 °C, indium(III) oksida bertukar kepada indium(I) oksida, In2O dan terurai pada 2000 °C. Sebatian ini larut dalam asid tetapi tidak dalam alkali.[2] Pada suhu tinggi, indium(III) oksida bertindak balas dengan ammonia untuk membentuk indium nitrida.[3]
Penggunaan
[sunting | sunting sumber]Dalam bidang elektronik, indium(III) oksida digunakan dalam semikonduktor sebagai semikonduktor jenis-n dan sebagai unsur perintang dalam litar bersepadu.[4]
Rujukan
[sunting | sunting sumber]- ^ Marezio, M. (1966). "Refinement of the crystal structure of In2O3 at two wavelengths". Acta Crystallographica. 20 (6): 723–728. doi:10.1107/S0365110X66001749.
- ^ a b Downs, Anthony John (1993). Chemistry of aluminium, gallium, indium, and thallium. Springer. ISBN 0-7514-0103-X.
- ^ Wiberg, Egon and Holleman, Arnold Frederick (2001) Inorganic Chemistry, Elsevier ISBN 0123526515
- ^ "In2O3 (Indium Oxide)". CeramicMaterials.info. Diarkibkan daripada yang asal pada 2008-06-30. Dicapai pada 2008-10-29.


