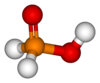
Asid hipofosforus
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Asid fosfinik
| |||
| Nama lain
Asid hidroksi(okso)-λ5-fosfana
hidroksi-λ5-fosfanona | |||
| Pengecam | |||
| |||
Imej model 3D Jmol
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.026.001 | ||
| KEGG | |||
PubChem CID
|
| ||
| Nombor PBB | UN 3264 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| H3PO2 | |||
| Jisim molar | 66.00 g/mol | ||
| Rupa bentuk | hablur atau cecair berminyak tanpa berwarna dan berlembap cair | ||
| Ketumpatan | 1.493 g/cm3[2] | ||
| Takat lebur | 26.5 °C (79.7 °F; 299.6 K) | ||
| Takat didih | 130 °C (266 °F; 403 K) | ||
| tercampur | |||
| Keterlarutan | sangat terlarut dalam alkohol, eter | ||
| Keasidan (pKa) | 1.2 | ||
| Struktur | |||
| Bentuk molekul | pseudo-tetrahedron | ||
| Bahaya | |||
| Takat kilat | Tidak mudah terbakar | ||
| Sebatian berkaitan | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Asid hipofosforus merupakan suatu oksoasid fosforus dan suatu agen penurun yang kuat dengan formula molekulnya H3PO2. Ahli kimia bukan organik merujuk asid bebas ini dengan nama ini (juga dengan singkatan "HPA"), atau dengan nama lain yang diterima asid fosfinik. Ia adalah sebatian leburan rendah yang tidak berwarna, yang larut dalam air, dioksana, dan alkohol. Formula untuk asid hipofosforus biasanya ditulis sebagai H3PO2, tetapi dalam bentuk pembentangan yang lebih deskriptif adalah HOP(O)H2 yang menonjolkan sifat monoprotiknya. Garam yang diperolehi daripada asid ini dipanggil sebagai fosfinat (hipofosfit).
HOP(O)H2 wujud dalam keseimbangan dengan tautomer minornya HP(OH)2. Kadang-kadang tautomer yang kecil dipanggil asid hipofosforus dan tautomer utama dipanggil asid fosfinik.
Penyediaan dan ketersediaan
[sunting | sunting sumber]Asid ini disediakan secara industri melalui satu proses dua langkah. Garam hipofosfit beralkali dan logam alkali bumi merupakan hasil dari rawatan fosforus putih dengan larutan akueus panas hidroksida bersesuaian, seperti Ca(OH)2.
- P4 + 3OH− + 3H2O → 3H2PO2− + PH3
Asid bebas boleh disediakan melalui tindakan asid yang kuat ke atas garam hipofosfit.
- H2PO2− + H+ → H3PO2
Sebagai alternatif, H3PO2 timbul melalui pengoksidaan fosfina dengan iodin dalam air.
- PH3 + 2I2 + 2H2O → H3PO2 + 4I− + 4H+
HPA biasanya dibekalkan sebagai larutan akueus 50%.
Sumber
[sunting | sunting sumber]- ChemicalLand21 Listing Diarkibkan 2013-01-02 di archive.today
- D. E. C. Corbridge "Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology" 5th Edition Elsevier: Amsterdam. ISBN 0-444-89307-5.
- V. V. Popik, A. G. Wright, T. A. Khan, J. A. Murphy "Hypophosphorous Acid" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. doi:10.1002/047084289.
- D. W. Rich, M. C. Smith, Electroless Deposition of Nickel, Cobalt & Iron. IBM Corporation, Poughkeepsie, NY (1971)
Rujukan
[sunting | sunting sumber]- ^ Ralph H. Petrucci, General Chemistry, Ninth Edition, 2007, p. 946
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8